1 무료
PPWR 2026, 기업이 지금 먼저 만들어야 하는 건 완성본이 아니라 TD/DoC 작성 체계다
1 멤버
PPWR TD 작성 로드맵 — Annex VII 기준으로 목차를 어떻게 잡아야 하나
2 멤버
PPWR DoC 작성 템플릿 — Annex VIII 기준으로 누가 어떤 문구로 선언해야 하나
3 멤버
공급업체 자료요청표 + 내부 체크리스트 — TD/DoC를 완성하기 위해 실제로 받아야 할 자료는 무엇인가


1 무료
PPWR 2026, 기업이 지금 먼저 만들어야 하는 건 완성본이 아니라 TD/DoC 작성 체계다
1 멤버
PPWR TD 작성 로드맵 — Annex VII 기준으로 목차를 어떻게 잡아야 하나
2 멤버
PPWR DoC 작성 템플릿 — Annex VIII 기준으로 누가 어떤 문구로 선언해야 하나
3 멤버
공급업체 자료요청표 + 내부 체크리스트 — TD/DoC를 완성하기 위해 실제로 받아야 할 자료는 무엇인가


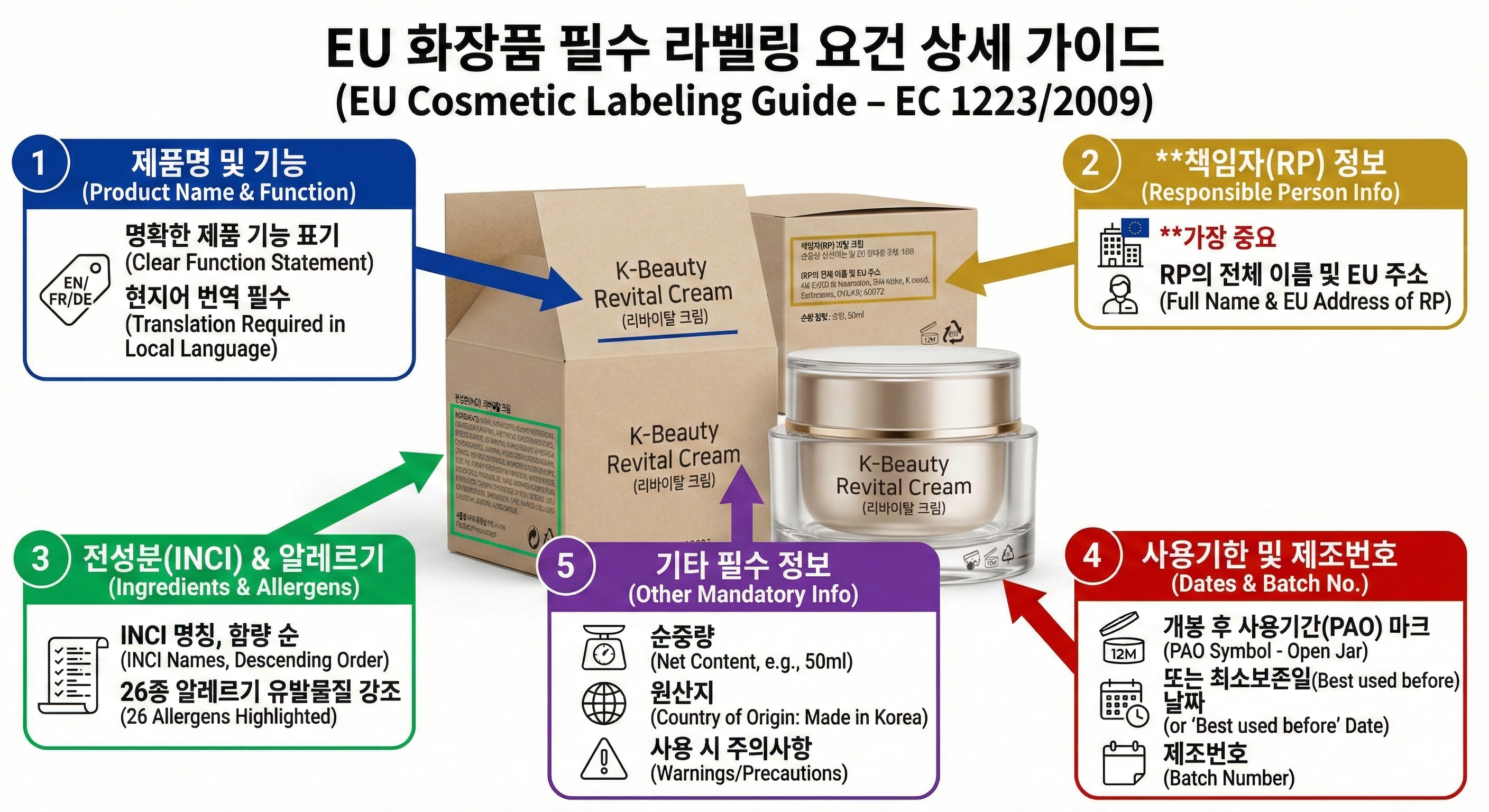

핵심 요건 1: 책임자 (RP - Responsible Person)
EU 내에 소재한 법인 또는 개인이어야 합니다. 수입업자, 유통업자가 될 수도 있고, 전문 RP 대행사를 지정할 수도 있습니다. 제품의 안전성 및 법적 문제에 대해 모든 법적 책임을 집니다.
핵심 요건 2: 제품 정보 파일 (PIF - Product Information File)
제품의 안전성을 입증하는 방대한 서류철입니다. 가장 핵심은 전문가(독성학자, 약사 등)가 서명한 **안전성 보고서(CPSR)**입니다.
핵심 요건 3: CPNP (Cosmetic Products Notification Portal)
제품을 시장에 출시하기 전, RP가 EU 위원회 온라인 포털에 제품 정보를 등록(Notification)하는 절차입니다.
1단계: 사전 준비 및 RP 지정 (수출 4~6개월 전)
가장 먼저 EU 현지에서 내 제품을 책임져 줄 대리인을 찾고, EU 기준에 맞는 성분인지 검토해야 합니다.
1-1. 책임자(RP) 지정 및 계약
전문 RP 서비스 대행사와 계약하거나, 역량이 충분한 현지 수입 바이어를 RP로 지정하고 위임장(Mandate)을 작성합니다.
1-2. 성분 사전 검토 (Formula Review)
EU 규정 부속서(Annexes)를 바탕으로 금지 원료, 제한 원료, 색소, 보존제, 자외선 차단제 기준에 적합한지 꼼꼼히 검토합니다. (특히 나노 물질 사용 시 6개월 전 사전 신고 필수)
동물실험 전면 금지: 완제품 및 원료에 대한 동물실험 데이터는 사용할 수 없습니다.
2단계: PIF 준비 및 CPSR 발급 (수출 3~5개월 전) [최대 난관]
EU 수출의 성패를 가르는 가장 중요하고 비용/시간이 많이 드는 단계입니다. RP가 지정한 안전성 평가사(Safety Assessor)의 엄격한 심사를 통과해야 합니다.
2-1. PIF (제품 정보 파일) 자료 취합
제조사는 다음 자료를 영문으로 준비해 RP에게 전달해야 합니다.
전성분표 (INCI 기준, 정확한 함량 및 CAS/EC 번호)
원료 MSDS, COA, 불순물/중금속 데이터
완제품 기준 및 시험방법, 안전성/안정성(유통기한) 시험 데이터, 방부력 테스트(PET), 용기 적합성 데이터
GMP(ISO 22716 등) 인증서
2-2. 화장품 안전성 보고서 (CPSR - Cosmetic Product Safety Report) 작성
Part A (안전성 정보): 취합된 데이터를 바탕으로 한 독성 및 안전성 정보.
Part B (안전성 평가): 자격을 갖춘 평가사가 Part A를 검토하여 "이 제품은 인체에 안전하다"고 최종 서명한 보고서. 이 서명이 있어야만 수출이 가능합니다.
3단계: 라벨링 및 클레임 검토 (수출 2~3개월 전)
3-1. EU 라벨링 규정 준수
필수 표기: RP의 상호 및 주소(EU 내), 원산지(한국), 순중량, 개봉 후 사용기간(PAO - 뚜껑 열린 통 마크) 또는 사용기한, 제조번호(Batch 번호), 기능/용도, 전성분(INCI), 경고 문구.
라벨은 판매되는 해당 국가의 공식 언어로 번역되어야 합니다.
3-2. 효능 클레임 (Claims) 검토
"주름 개선", "보습" 등의 문구를 사용하려면 이를 과학적으로 입증할 수 있는 효능 평가(임상 등) 자료가 PIF에 포함되어 있어야 합니다. 허위/과대광고 규제가 엄격합니다.
4단계: CPNP 온라인 등록 (수출 1개월 전)
PIF와 라벨이 모두 완성되면 마무리하는 신고 단계입니다.
4-1. CPNP 포털 등록
RP가 CPNP 시스템에 접속하여 제품의 라벨, 패키지 사진, 전성분, 중독관리센터(Poison Centre) 대응을 위한 처방 정보 등을 업로드합니다.
등록이 완료되면 **CPNP Reference Number(등록 번호)**가 발급됩니다. 별도의 승인 대기 시간은 없습니다(업로드 즉시 유효).
5단계: 선적 및 수출 (수출 직전 및 사후 관리)
5-1. 통관
발급받은 CPNP 번호와 함께 필수 선적 서류를 갖춰 수출합니다. 세관에서 RP 정보와 라벨을 대조 확인합니다.
5-2. 시장 유통 및 사후 관리
RP는 제품이 단종된 후에도 10년간 PIF를 최신 상태로 보관하고, 보건 당국의 요청 시 즉각 제출할 의무가 있습니다.
심각한 부작용(SUE) 발생 시 RP는 즉시 당국에 보고해야 합니다.
EU 화장품 수출 Tip
시간과 예산의 여유: PIF 작성과 특히 CPSR(안전성 보고서) 발급은 매우 까다로워 예상치 못한 지연(원료 데이터 부족, 용기 호환성 테스트 누락 등)이 빈번하게 발생합니다. 최소 6개월의 넉넉한 준비 기간이 필요합니다.
용기(Packaging) 데이터 필수: 내용물뿐만 아니라 화장품을 담는 플라스틱/유리 용기에 대한 중금속 불검출 및 호환성 데이터도 엄격하게 요구됩니다.
영국 수출(UKCA/UKCPNP): 브렉시트 이후 영국은 자체적인 UKCPNP 시스템과 별도의 영내 RP를 요구합니다. EU를 준비했다면 서류(PIF)는 그대로 쓸 수 있으나, 시스템 등록과 RP 지정은 영국용으로 한 번 더 해야 합니다.
와이에스엠경영컨설팅 윤수만